Сравнительное изучение внутрипузырной инстилляции химиотерапевтического препарата в сочетании с гипертермией и внутрипузырной химиотерапии для профилактики рецидивов поверхностного переходноклеточного рака мочевого пузыря (STCCB).
Целью данного исследования было сравнение эффективности инстилляции химиотерапевтического агента в сочетании с местной гипертермией выполненное системой Synergo ® с инстилляцией химиотерапевтическими агентами.
Пациентам со средним и высоким риском (в основном, рецидив после предыдущего лечения, включая БЦЖ) был выполнен ТУР мочевого пузыря. В качестве химиотерапевтического агента в исследовании применялся МитомицинС .
Работа была разделено на два рандомизированных исследования.
В исследовании участвовали медицинские центры:
больница Сан Раффаэле, Милан, Италия; Университетский госпиталь, Палермо, Италия; Медицинский центр Рабина, Бейлинсон Кампус. Петах-Тиква, Израиль.
| I группа |
Внутрипузырная химиотерапия совместно с местной гипертермией — Synergo ®
|
| II группа |
Внутрипузырная химиотерапия
|
Время наблюдения от 2 до 5 лет
Анализ эффективности:
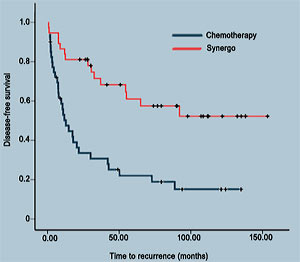
На следующем графике представлены результаты безрецидивной выживаемости, по Каплан-Мейеру:
Долгосрочные результаты ? за 24 месяцев (до 5 лет) наглядно демонстрируют статистически значимую (р = 0,0006) разницу в частоте возникновения рецидивов между двумя группами: в внутрипузырные химиотерапии группе (65%) по сравнению с группой Synergo ® (25,7%).
Побочные эффекты
Большинство побочных эффектов были общими для этих двух групп пациентов:
дизурия, кожная аллергия на митомицин, гематурия. Единственным различием была неострая боль во время сеанса гипертермиии (временная, поверхностная, проходящая без медицинского вмешательства).
Рецидив
За весь период наблюдений у 35 пациентов были зарегистрированы случаи рецидива опухоли, 9 в группе Synergo ® и 26 в группе внутрипузырной химиотерапии.
Опыт профилактического лечения с помощью Synergo, накопленный в период до 2006 года
Как это часто бывает, в начале реализации новых медицинских технологий, большинство пациентов, направленных на профилактическое лечение Synergo были самыми трудными, которые исчерпали все возможности альтернативного лечения.
В этом отчете мы сообщаем о нашем опыте адъювантного лечения с Synergo 131 пациента в следующих центрах:
| Италия: | HSR Hospital, Milan; University Policlinic Hospital, Palermo; IEO hospital, Milan; Galliera Hospital, Genoa Treviglio Hosptial, Treviglio; Magenta Hospital, Magenta; Humanitas Gavazzeni, Bergamo |
| Израиль: | Bnai Zion Hospital, Haifa; Wolfson Medical Center, Holon; Rabin Medical Center, Belinson Campus, Petah-Tikva; Hadassah Medical Center, Jerusalem; Meir Medical Centre, Kefar-Saba; Carmel Hospital, Haifa |
| Германия: | Muenchen-Harlaching (Krankenhaus), Munich; City Hospital, Offenbach |
| Нидерланды: | UMC St Radboud, Nijmegen; Academic Hospital, Maastricht |
| Австрия: | Clinic Innsbruck |
| Франция: | Hopital d’instruction des armees du Val de Grace, Paris; Tenon Hospital, Paris |
Пациенты:
Возраст: Средний: 67 Диапазон: 32-98
Пол: 105 мужчин (80%) 26 женщин (20%)
Высокий риск: 63%
Средний риск: G1: 37%
У пациентов с высоким риском (83) до сеансов Синерго в среднем было 3,4 случая рецидива.
На пациента со средним риском (48) приходилось в среднем 3,2 рецидива до сеансов Синерго. В среднем безрецидивный интервал для этой группы составлял 362 дней.
Среднее значение рецидивов: 3,4
Число больных с 3 или более рецидивами за предшествующие 24 месяца: 26 (19,8%) (высокий рецидив)
Число пациентов, которые ранее подверглись БЦЖ терапии: 37 (28%)
Число пациентов, которые ранее подверглись внутрипузырной химиотерапии: 73 (56%)
Результаты
1. Результаты 131 пациента с профилактическим лечением:
У 28 пациентов был рецидив (20,0%)
Пациенты с высоким риском: 21 рецидив (25%), 2-летняя безрецидивная оценка по Каплану-Мейеру 60%
Пациенты со средним риском: 7 случаев рецидива (14,5%), 2-летняя безрецидивная оценка по Каплану-Мейеру 69%.
2. Прогрессия рака Т в T1 наблюдалась только у 2 больных после 13 месяцев наблюдений (диапазон 2-66 месяцев)
3. Побочные эффекты:
Неострая боль во время сеанса, дизурия, гематурия и частые позывы к мочеиспусканию в первые сутки после окончания лечения. Все пациенты возобновили нормальную повседневную деятельность сразу после процедуры.
Synergo аблятивное лечение, опыт, накопленный в период до 2006 года
Пациенты с обширной опухолью и / или мультифокальной опухолью, CIS, для которых не возможно удаление опухоли во время одной операции, пациенты, которым предложена цистэктомия.
В настоящем исследование приведен опыт аблятивного лечения 219 пациентов со средним и высоким риском STCCB (85% с высокой степенью риска, 15% пациентов со средней степенью риска), пролеченных в следующих центрах:
| Италия: | HSR Hospital, Milan; University Policlinic Hospital, Palermo; IEO hospital, Milan; Galliera Hospital, Genoa; ; Treviglio Hosptial, Treviglio; Magenta Hospital, Magenta; Humanitas Gavazzeni, Bergamo; Ascoli-Piceno Hospital |
| Израиль: | Bnai Zion Hospital, Haifa; Wolfson Medical Center, Holon; Hadassah Medical Center, Jerusalem Rabin Medical Center, Belinson Campus, Petah-Tikva; Meir Medical Centre, Kefar-Saba; Carmel Hospital, Haifa |
| Германия: | Mannheim University Hospital; Muenchen-Harlaching (Krankenhaus), Munich |
| Нидерланды: | UMC St Radboud, Nijmegen |
| Франция: | St. Louis Hospital, Paris |
Характеристика пациентов:
219 пациентов с высокими средним риском STCCB (85% с высокой степенью риска, 15% пациентов со средним).
Возраст: Средний: 70 лет Диапазон: 37-97
Пол: 162 мужчин (74%) 57 женщин (26%)
Число пациентов, которые ранее подверглись БЦЖ терапии: 119 (54%)
Число пациентов, которые ранее подверглись химиотерапии: 156 (71%)
Продолжительность безрецидивного интервала определялся с помощью видео-цистоскопии каждые 3 месяца в течение 2 лет. Выполнялись биопсии и цитологии мочи. Начало интервала свободного от болезни определялся в момент полного искоренения опухоли.
Во многих случаях, безрецидивное состояние было вызвано лечением Synergo ®; у некоторых пациентов потребовалась дополнительная операция. CR (полный ответ) — Нет признаков заболевания следующие Synergo лечении ПР (Частичная Response) — уменьшение> 50% объема опухоли NC (без изменений) — опухоль unchanhed или только слегка сократилось в том длину болезней свободное время после полного нищеты, был записан.
Результаты
1. Результаты наблюдений:
У 175 из 216 пациентов (80%) аблятивное лечение с помощью технологии Synergo ® вызвало полную ликвидацию опухолей
У 31 пациента (14%) было выявлено уменьшение опухоли после чего стало возможно проведение ТУР.
13 из 219 пациентов (6%) не отреагировали на лечение.
2. Побочные эффекты:
Неострая боль во время сеанса, дизурия, гематурия и частые позывы к мочеиспусканию в течение первых нескольких дней после лечения. Уменьшение объема пузыря произошло у 3 (1,4%) пациентов. Все пациенты возобновили нормальную повседневную деятельность после каждой процедуры.
Выводы
Synergo ® технология является высокоэффективным и безопасным методом лечения, достигающий в 80% полного излечения. Synergo является вариантом лечения для пациентов с рецидивом после БЦЖ или внутрипузырной химиотерапией.
Рандомизированное контролируемое исследование лечения с помощью системы Synergo ® гипертермия в сочетании с Митомицином C по сравнению с внутрипузырной иммунотерапией (БЦЖ) у пациентов с переходным поверхностным раком мочевого пузыря
Текущие клинические исследования Медикал Энтепрайз начались в 2002 году. Это рандомизированное многоцентровое исследование. В исследовании участвуют урологические отделения больниц Италии, Франции, Нидерландов, Бельгии и Израиля.
Главный исследователь:
Проф.Дж.А.Уайтджес, Кафедра урологии, госпиталь Радбаундского (Radbound) Университета, Нидерланды
Участники исследования:
- Пациенты с поверхностным раком мочевого пузыря (Та, T1 или CIS) после трансуретральной резекции (ТУР).
- Средний или высокий риск рецидива или прогрессии.
- Не было внутрипузырных инстилляций Митомицина С в последние 12 месяцев, или БЦЖ в последние 24 месяца
Для получения дополнительной информации о клиническом исследовании, а также список участвующих медицинских центров пожалуйста свяжитесь с нами.